技术小站 | 细胞因子释放综合症
细胞因子释放综合症(Cytokine Release Syndrome, CRS)也被称为细胞因子风暴(Cytokine Storm),是一种因免疫细胞被激活 并释放大量细胞因子而引发的严重全身炎症反应综合症,临床表现包括发热、寒颤、恶心、呕吐、低血压、呼吸急促、头疼等,严重可能导致多器官衰竭和死亡。
发生机制
可溶性抗体通过抗原决定簇
可溶性抗体通过抗原决定簇(Complementarity Determining Regions, CDRs)直接结合至效应细胞表面的同源受体上,直接激发效应细胞释放大量细胞因子。
可溶性抗体与效应细胞表面同源受体结合
可溶性抗体与效应细胞表面同源受体结合,并与已存在的抗IgG抗体交叉结合,引起效应细胞激活并释放细胞因子。
可溶性抗体微弱地结合在效应细胞表面
可溶性抗体微弱地结合在效应细胞表面,通过Fc与邻近非效应细胞表面FcR结合,引起效应细胞表面抗原聚集,刺激效应细胞释放细胞因子。
可溶性抗体结合至效应细胞
可溶性抗体结合至效应细胞,通过Fc与临近的非效应细胞表面FcR交叉结合,激活非效应细胞(含有FcR的细胞)释放大量细胞因子。由于人体免疫系统的复杂性,体内CRS可能由多种机制共同参与导致。
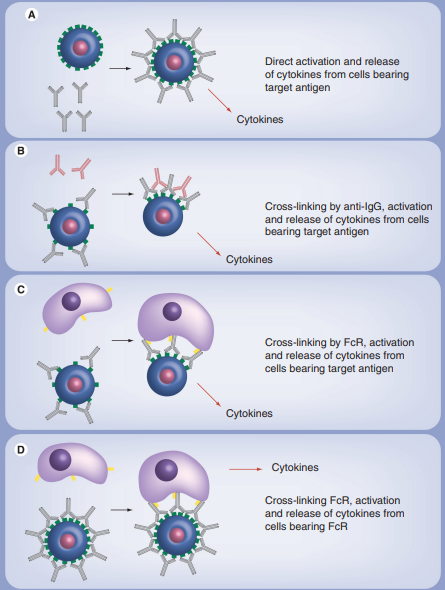
图一 CRS发生机制
CRS经典案例
TGN1412是一款靶向T细胞的共刺激受体CD28的超级激动剂,在2006年,该抗体第一次进入人体临床实验时,6个受试者在注射该抗体的90分钟内,便产生了严重危及生命安全的细胞因子风暴。
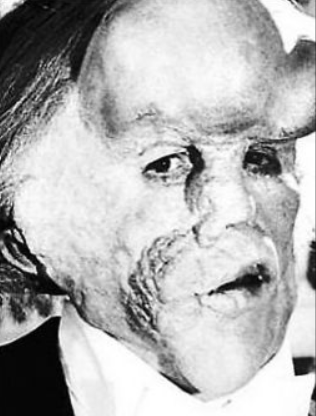
图二 TGN1412受害者影像记录
事后的分析确认用于临床实验抗体的成品是符合标准规范的,尤其是排除了可能引起细胞因子风暴成因的内毒素的污染。这说明在临床前研发阶段TGN1412的免疫毒性实验结果对人体内的安全性预测失败。这些临床前的实验包括体外试验评估,即体外人和其他物种的PBMC / 全血细胞进行细胞因子释放的测定,也包括体内试验评估,即亲缘相近的灵长类哺乳动物食蟹猴的体内实验测定细胞因子释放。当前的体外实验和体内动物模型具有局限性,尚未能准确识别具有CRS不良反应的药物,且不能可靠预测药物在人体应用时的发生、发展,因此,探寻优化的体外细胞因子释放实验(Cytokine Release Assays, CRA)成为临床前安全性评价的研究热点。
CRA实验怎么做
NIBSC在2020年组织了国际上知名大药企,包括Amgen, Pfizer, Roche,GSK,BMS等共同进行了一次能力测评和国际协作研究,并选定了CD3抗体OKT3, CD28抗体TGN1412, CD52抗体Campath-1H作为测评的阳性药物。
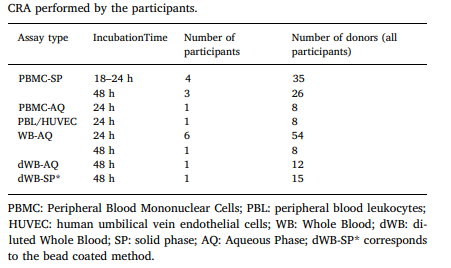
图三 TGN1412体外试验的6种模型
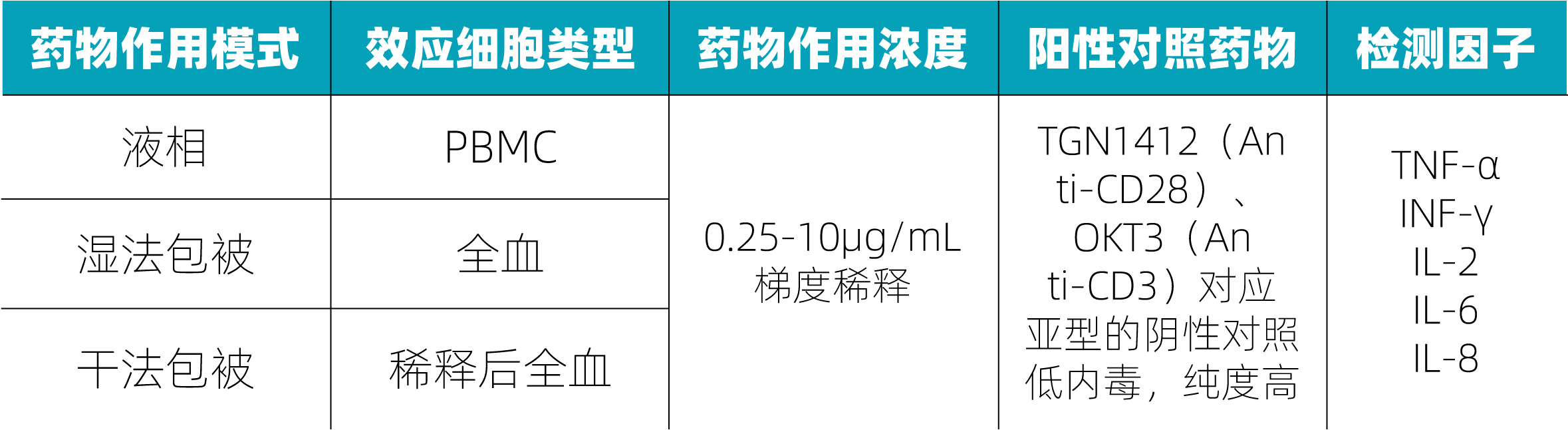
图四 澳能生物免疫调节剂体外细胞因子室验模型要素
数据展示

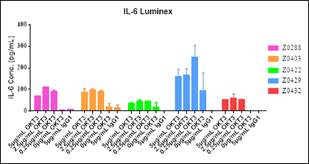
图五 按照Oricells实验设计要求,梯度稀释的OKT3与不同志愿者来源的冻存PBMC共孵育48小时后,使用Luminex检测各因子分泌情况。上图为部分因子结果展示。
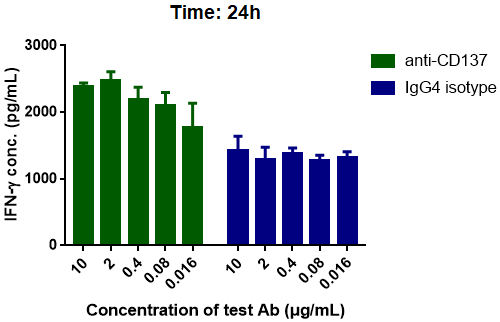
图六 使用0.1μg/ml CD3与CD137共刺激24小时,检测IFN-γ因子分泌
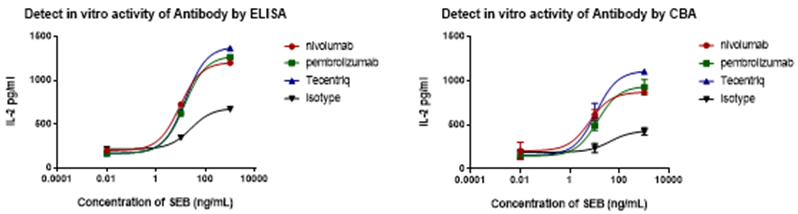
图七 T细胞活化通过暴露于特定抗原后测定(例如葡萄球菌肠毒素B,SEB)
欢迎各位老师前来咨询!